问题
问答题
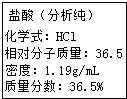
实验室一分析纯盐酸的标签如图所示;某钢铁厂为了 测定赤铁矿中Fe2O3的含量,将20g赤铁矿(杂质既不与酸 反应也不溶于水)加到219g10%的稀盐酸中,恰好完全反应 生成氯化铁和水.求:
(1)Fe2O3中铁元素与氧元素的质量比为______;
(2)欲配制219g 10%的稀盐酸,需用这种分析纯盐酸______g;
(3)求赤铁矿中含Fe2O3的质量分数.
答案
(1)根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,所以氧化铁中,铁元素和氧元素的质量比为:
56×2:16×3=7:3,故答案为:7:3;
(2)根据稀释前后溶质的质量不变,设配制219g 10%的稀盐酸,需用这种分析纯盐酸 x g,则可列式为:
219g×10%=x×36.5% 解答x=60 g; 故答案为:60 g;
(3)设与219g10%的稀盐酸恰好完全反应的Fe2O3的质量为 y g
Fe2O3 +6HCl=FeCl3+H2O
160 219
y 219g×10%
=160 219 y 219g×10%
y=16g,
根据物质纯度=
×100%,则赤铁矿中含Fe2O3的质量分数=纯净物质量 混合物质量
×100%=80%.16 20
故答案为:80%.
