据报道,有一种叫Thibacillus Ferroxidans的细菌在氧气存在下的酸性溶液中,能将黄铜矿(CuFeS2)氧化成硫酸盐,发生的反应为:4CuFeS2+2H2SO4+17O2=4CuSO4+2Fe2(SO4)3+2H2O
(1)CuFeS2中Fe的化合价为+2,上述反应中被氧化的元素是________。
(2)工业生产中利用上述反应后的溶液,按如下流程可制备胆矾(CuSO4·5H2O)
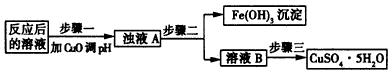
①分析下列表格(其中Ksp是相应金属氢氧化物的沉淀溶解平衡常数)
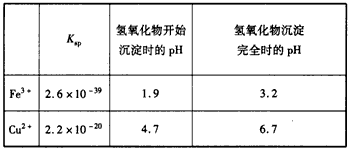
运用沉淀溶解平衡的有关理论解释加入CuO能除去CuSO4溶液中Fe3+的原因__________________;
②步骤三中的具体操作方法是____________________。
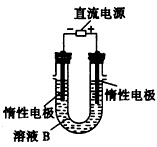
(3)有人提出可以利用如图的装置从溶液B中提炼金属铜。该过程中右边电极的反应式是____________,总反应方程式是____________________。
(4)工业上冶炼铜的方法之一为:Cu2S(s)+2Cu2O(s)= 6Cu(s)+SO2(g) △H
已知:
①2Cu(s)+1/2O2(g)=Cu2O(s) △H=-12 kJ/mol
②2Cu(s)+S(s)=Cu2S(s) △H=-79.5 kJ/mol
③S(s)+O2(g)=SO2(g) △H=-296.8 kJ/mol
则该法冶炼铜的反应中△H=________。
(1)Fe、S或铁、硫
(2)①3.2≤pH<4.7;加入CuO与H+反应使c(H+) 减小,c(OH-)增大,使溶液中c(Fe3+)·C3(OH-)>
Ksp[Fe(OH)3],导致Fe3+生成沉淀而除去;②蒸发浓缩,冷却结晶
(3)4OH--4e-=2H2O+O2↑;2CuSO4+2H2O 2Cu+2H2SO4+O2↑
2Cu+2H2SO4+O2↑
(4)-193.3 kJ/mol
