把18.0mol/L的浓硫酸稀释成1.80mol/L的稀硫酸100mL,实验操作如下:
(1)请在下列操作步骤中填写有关的空格:
①用量筒量取______mL的18.0mol/L的浓硫酸;
②将______沿烧杯内壁慢慢注入盛有少量______的烧杯中;
③将已冷却至室温的硫酸溶液沿玻璃棒注入______mL的容量瓶中;
④用少量蒸馏水洗涤烧杯2-3次,并将洗涤液也全部转移到容量瓶中;
⑤继续向容量瓶中加蒸馏水,直到液面接近刻度线______cm处;
⑥改用______逐滴加蒸馏水,使溶液凹面恰好与刻度相切;
⑦盖好容量瓶塞,反复颠倒,摇匀;
⑧将配好的稀硫酸倒入试剂瓶中,贴好标签.
(2)由于操作不当,会引起实验误差.下列情况对所配制的H2SO4溶液的物质的量浓度有何影响?______(用偏大、偏小、无影响填写):
①容量瓶用蒸馏水洗涤后残留有少量的水______;
②摇匀后,发现溶液的液面低于刻度线,又加水至刻度线______.
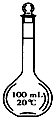
(3)容量瓶(如图)上标有______(选填下列编号)
①温度②浓度③容量④压强⑤刻度线.
(1)配制1.80mol/L的稀硫酸100mL,需要18.0mol/L的浓硫酸的体积为:
=0.01L=10mL,所以应该选用10.0mL的量筒;稀释浓硫酸时,应该将浓硫酸沿着烧杯内壁慢慢注入蒸馏水中,顺序不能颠倒;配制100mL溶液需要选用100mL容量瓶;定容时先直接加入蒸馏水,至容量瓶刻度线1-2cm时,改用胶头滴管进行定容;1.8mol.L×0.1L 18mol/L
故答案为:10.0;浓硫酸;蒸馏水;100mL;1-2cm,胶头滴管;
(2)①容量瓶用蒸馏水洗涤后残留有少量的水,对溶液体积和溶质的物质的量都不产生影响,所以不影响配制结果,
故答案为:无影响
②摇匀后,发现溶液的液面低于刻度线,又加水至刻度线,导致配制的溶液体积偏大,溶液的浓度偏小,
故答案为:偏小;
(3)容量瓶是一种定量仪器,由于配制一定体积的溶液,所以容量瓶上标有刻度线、容量,温度影响溶液的体积,所以容量瓶上还标有温度,
故答案为:①③⑤.
