下图所示是实验室中制取气体时常用装置。请回答下列问题:
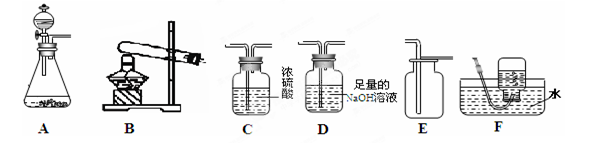
(1)在实验室中制取气体时,加入药品之前一定要先检验 。
(2)以石灰石和稀盐酸为原料制取并收集干燥的CO2气体。
①各装置的正确连接顺序是(填装置序号) 。
②产生CO2气体的化学方程式为 。
③C装置的作用是 。
④检验集气瓶中是不是CO2气体的方法 。
(3)同学甲为验证制取CO2后剩余溶液中是否含有盐酸(杂质不溶于水且不参加反应,且CaCl2溶液呈中性),设计实验方案如下:取样于试管中,滴加AgNO3溶液,产生白色沉淀,再加入稀硝酸,沉淀不溶解,则含有盐酸。你是否同意该方案?简述理由。 。
(4)将少量CO2气体通入盛有足量Ca(OH)2溶液的广口瓶中,瓶中溶液的质量与之前相比会 (填写下列各项序号)。
A.增大
B.减小
C.不变
D.无法判断
(1)装置的气密性
(2)①ACE;②CaCO3+2HCl=CaCl2+2H2O+CO2↑;③干燥气体或吸收气体中的水分;④加入少量的澄清石灰水并振荡,若看到澄清的石灰水变浑浊,则是CO2;
(3)不同意,因为剩余溶液中一定含有CaCl2,不管是否有稀盐酸,滴加AgNO3都会产生不溶于稀硝酸的白色沉淀;
(4)A
题目分析:(1)在实验室制取气体时,加入药品之前一定要先检验装置的气密性,以防生成的气体逸出;(2)①实验室用大理石和稀盐酸反应制取二氧化碳,反应物的状是固体和液体,反应条件是常温,应选用发生装置A;由于二氧化碳的密度大于空气的密度,可选用收集装置B;在收集前用浓硫酸进行干燥,所以可采用的装置组合是ACE;②实验室制取CO2用大理石和稀盐酸,化学方程式为:CaCO3 +2HCl═CaCl2+H2O+CO2↑;③浓硫酸具有吸水性,所以可用来干燥气体或吸收气体中的水分;④检验CO2气体的方法加入少量的澄清石灰水并振荡,若看到澄清的石灰水变浑浊,则是CO2;
(3)溶液中一定含有CaCl2,不管是否有稀盐酸,都能和AgNO3溶液反应生成不溶于稀硝酸的白色沉淀,因此该方案不完善;
(4)二氧化碳能和氢氧化钠反应生成碳酸钠和水,因此将少量CO2气体通入盛有足量NaOH溶液的广口瓶中,瓶中溶液的质量与之前相比会增加;故选A
