问题
选择题
将0.15 mol Fe3O4完全溶解在足量稀硫酸中,然后加入K2Cr2O7溶液250 mL,恰好使溶液中Fe2+全部氧化成Fe3+,Cr2O72-全部转化成Cr3+,则K2Cr2O7溶液的物质的量浓度是
A.0.05 mol/L
B.0.1 mol/L
C.0.2 mol/L
D.0.3 mol/L
答案
答案:B
题目分析:根据Fe3O4+4H2SO4=FeSO4+Fe2(SO4)233+4H2O 可知,Fe2+含有0.15mol,再根据6Fe2++14H++Cr2O72-=6Fe3+2Cr3++7H2O , Cr2O72-需要的物质量就为0.025mol,故K2Cr2O7溶液的物质的量浓度为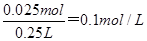 ,答案选B。
,答案选B。
点评:本题考查物质的量浓度计算,属于易错题,计算过程应注意化学方程式的书写。
