问题
选择题
标准状况下有①6.72LCH4 ②3.01×1023个HCl分子 ③13.6gH2S ④0.2molNH3,下列对四种气体的关系从小到大表示不正确的是( )
A.密度: ①<④<③<②
B.体积:④<①<②<③
C.质量: ④<①<③<②
D.氢原子数: ②<④<③<①
答案
答案:B
题目分析:根据阿伏伽德罗定律的推论:同温同压下,密度之比等于相对分子质量之比,所以密度关系为:①<④<③<②,故A正确;3.01×1023个HCl的体积V=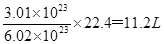 、
、
13.6gH2S的体积V=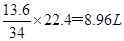 、0.2molNH3的体积V=0.2mol×22.4L/mol═4.48L,所以体积关系为:④<①<③<②,故B不正确;6.72LCH4的质量是m=
、0.2molNH3的体积V=0.2mol×22.4L/mol═4.48L,所以体积关系为:④<①<③<②,故B不正确;6.72LCH4的质量是m=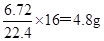 、3.01×1023个HCl的质量为0.5mol×36.5g/mol=18.25g,0.2molNH3的质量是0.2mol×17g/mol=3.4g,所以质量关系是④<①<③<②,故C正确;6.72LCH4的物质的量为0.3mol,所以氢原子的物质的量为1.2mol,3.01×1023个HCl的物质的量为0.5mol,所以氢原子的物质的量为0.5mol,13.6gH2S的物质的量为0.4mol,所以氢原子的物质的量为0.8mol,0.2molNH3氢原子的物质的量为0.6mol,氢原子数目和氢原子的物质的量成正比,所以氢原子数关系是②<④<③<①,故D正确,答案选B。
、3.01×1023个HCl的质量为0.5mol×36.5g/mol=18.25g,0.2molNH3的质量是0.2mol×17g/mol=3.4g,所以质量关系是④<①<③<②,故C正确;6.72LCH4的物质的量为0.3mol,所以氢原子的物质的量为1.2mol,3.01×1023个HCl的物质的量为0.5mol,所以氢原子的物质的量为0.5mol,13.6gH2S的物质的量为0.4mol,所以氢原子的物质的量为0.8mol,0.2molNH3氢原子的物质的量为0.6mol,氢原子数目和氢原子的物质的量成正比,所以氢原子数关系是②<④<③<①,故D正确,答案选B。
点评:在进行物质的量的有关计算时,关键是熟练应用几个关系式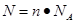 、n=m/M、
、n=m/M、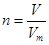 、
、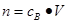 ,特别还要注意气体摩尔体积的使用条件,即只能适用于气体,且只有在标准状况下,气体的摩尔体积才是22.4L/mol。
,特别还要注意气体摩尔体积的使用条件,即只能适用于气体,且只有在标准状况下,气体的摩尔体积才是22.4L/mol。
