请完成下列填空:
(1)当SO2和SO3中分子个数比为1∶1 时,原子总数之比为 ,质量之比为 。
(2)中和含0.2 mol HCl的稀盐酸,需NaOH的质量为 g。
(3)现有m g某气体,它由双原子分子构成,它的摩尔质量为M g·mol—1,则:
①该气体的物质的量为 mol。
②该气体在标准状况下的体积为 L。
③该气体溶于水后形成V L溶液(不考虑反应),其溶液的物质的量浓度为 mol·L—1。
(4)将5 mol/L的Mg(NO3)2溶液a mL稀释至b mL,稀释后溶液中NO3-的物质的量浓度是 mol·L—1。
(5)用等体积的0.1 mol·L—1的BaCl2溶液,可使相同体积的Fe2(SO4)3、Na2SO4、KAl(SO4)2三种溶液中的SO42—完全沉淀,则三种硫酸盐的物质的量浓度之比为 。
(12分)
(1)3∶4 4∶5 (2)8 (3)①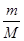 ②
②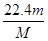 ③
③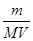 (4)10a/b mol/L (5)2∶6∶3
(4)10a/b mol/L (5)2∶6∶3
题目分析:(1)、设SO2和SO3中分子个数均为x个,则它们所含原子总数之比为(x+2x)∶(x+3x)=3∶4;由于n=N/NA,则它们的物质的量之比为1∶1 ,设均为ymol;由于m=n•M,则它们的质量之比为(64y)∶(80y)=4∶5;(2)、盐酸与氢氧化钠中和反应式为NaOH+HCl=NaCl+H2O,由于两反应物的化学计量数之比等于物质的量之比,则消耗NaOH的物质的量为0.2mol;由于m=n•M,则NaOH的质量为0.2mol×40g/mol=8g;(3)、①由于n=m/M,则该气体的物质的量为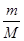 mol;②由于V=n×22.4L/mol,则该气体气体为
mol;②由于V=n×22.4L/mol,则该气体气体为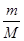 mol×22.4L/mol=
mol×22.4L/mol=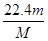 L;③由于c=n/V,则该气体溶解所得溶液中溶质的物质的量浓度为
L;③由于c=n/V,则该气体溶解所得溶液中溶质的物质的量浓度为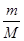 mol÷VL=
mol÷VL=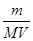 mol/L;(4)由稀释定律可知,稀释前后硝酸镁的物质的量相等,c1•V1=c2•V2,则稀释后硝酸镁的物质的量浓度为5a/bmol/L;硝酸镁的电离方程式为Mg(NO3)2=Mg2++2NO3—,生成物与反应物的化学计量数之比等于物质的量之比,则稀释后硝酸根离子浓度为10a/bmol/L;(5)、沉淀反应式均为Ba2++SO42—=BaSO4↓,两反应物的化学计量数之比等于物质的量之比,由于三反应消耗的氯化钡相同,设Ba2+和SO42—均为xmol;三种可溶性硫酸盐的电离方程式为:Fe2(SO4)3=2Fe3++3SO42—、Na2SO4=2Na++SO42—、KAl(SO4)2=K++Al3++2SO42—,其中反应物和硫酸根离子的化学计量数之比等于物质的量之比,则消耗的Fe2(SO4)3、Na2SO4、KAl(SO4)2分别为x/3mol、xmol、x/2mol;由于三种硫酸盐溶液体积相同,c=n/V,则Fe2(SO4)3、Na2SO4、KAl(SO4)2的物质的量浓度之比为x/3∶x∶x/2=2∶6∶3。
mol/L;(4)由稀释定律可知,稀释前后硝酸镁的物质的量相等,c1•V1=c2•V2,则稀释后硝酸镁的物质的量浓度为5a/bmol/L;硝酸镁的电离方程式为Mg(NO3)2=Mg2++2NO3—,生成物与反应物的化学计量数之比等于物质的量之比,则稀释后硝酸根离子浓度为10a/bmol/L;(5)、沉淀反应式均为Ba2++SO42—=BaSO4↓,两反应物的化学计量数之比等于物质的量之比,由于三反应消耗的氯化钡相同,设Ba2+和SO42—均为xmol;三种可溶性硫酸盐的电离方程式为:Fe2(SO4)3=2Fe3++3SO42—、Na2SO4=2Na++SO42—、KAl(SO4)2=K++Al3++2SO42—,其中反应物和硫酸根离子的化学计量数之比等于物质的量之比,则消耗的Fe2(SO4)3、Na2SO4、KAl(SO4)2分别为x/3mol、xmol、x/2mol;由于三种硫酸盐溶液体积相同,c=n/V,则Fe2(SO4)3、Na2SO4、KAl(SO4)2的物质的量浓度之比为x/3∶x∶x/2=2∶6∶3。