(1)37Cl—离子结构示意图 ,质量相等的两种物质SO2和SO3,所含氧原子个数之
为 ;
(2)20.6g NaR 含有Na+0.2mol,则NaR的摩尔质量为 ,则含R 8.0g 的NaR的物质的量为 ;
(3)在标准状况下,4.8g甲烷(CH4)所占的体积为_________L,它与标准状况下________L硫化氢(H2S)含有相同数目的氢原子;
(4)在100g浓度为18 mol·L-1、密度为ρ(g·cm–3)的浓硫酸中加入一定量的水稀释成9mol·L-1的硫酸,则加入水的体积 100mL(填“>”、“<”、“=”)
(1)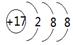 5: 6
5: 6
(2)103 g/mol(单位不写不得分); 0.1 mol
(3)6.72; 13.44
(4)<
题目分析:(1)Cl‾为18电子,第三层电子数为8;质量相等的两种物质SO2和SO3,所含氧原子个数之为m÷64×2:m÷80×3=5:6。
(2)Na+为0.2mol,则NaR为0.2mol,M(NaR)=20.6g÷0.2mol=103g/mol;由NaR的摩尔质量可得M(R)=80g/mol,则n(NaR)=n(R)=8.0g÷80g/mol=0.1mol。
(3)根据气体摩尔体积进行计算,V(CH4)=4.8g÷16g/mol×22.4L/mol=6.72L;4.8g÷16g/mol×4=V(H2S)÷22.4L/mol×2,可得V(H2S)=13.44L。
(4)由18 mol·L-1H2SO4稀释为9mol·L-1,应使溶液体积变为原来的2倍,因为硫酸溶液的密度随着浓度的减小而减小,稀释后的硫酸溶液质量小于原溶液的2倍,所以加入水的体积小于100ml。
