问题
问答题
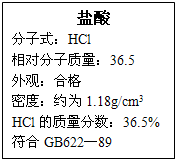
右图为某市售盐酸试剂瓶标签上的部分数据.通过计算回答:
(1)求该浓盐酸的物质的量浓度.
(2)用上述浓盐酸和二氧化锰加热反应制取氯气,若生成氯气的体积在标准状况下为4.48L时,则被氧化的HCl的质量为多少克?
答案
(1)盐酸的物质的量浓度为c=
=1000ρw M
mol/L=11.8moL/L,1000×1.18×36.5% 36.5
答:该浓盐酸的物质的量浓度为11.8mol/L;
(2)反应的方程式为MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O, △ .
根据方程式计算:
MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O △ .
4×36.5g 22.4L
m 4.48L
m=
=29.2g,4×36.5g×4.48L 22.4L
根据方程式和化合价的变化情况可知,被氧化的盐酸是参加反应的盐酸的一半,
所以被氧化的HCl的质量为
=14.6g,29.2g 2
答:被氧化的HCl的质量为14.6g.
