图是元素周期表的框架
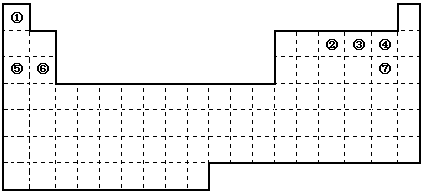
(1)请在上面元素周期表中画出金属元素与非金属元素的分界线。
(2)依据元素周期表回答下列问题:
A.周期表中的元素⑤和元素⑥的最高价氧化物的水化物碱性强弱顺序是____________(用化学式表示)。
B.周期表中的元素④和元素⑦的氢化物的熔、沸点高低顺序是____________(用化学式表示)。
C.①~⑦元素的单质,在常温下化学性质稳定,通常可用作保护气的是__________(填写分子式)。
D.在上面元素周期表中全部是金属元素的主族是__________;全部是非金属元素的主族是________(填写字母a、b、c、d)。
a.ⅠA族 b. ⅡA族 c. ⅥA 族 d.ⅦA族
(3)已知甲元素位于第三周期,且其原子半径为同周期金属元素中原子半径最小的,请写出甲的氧化物与NaOH溶液反应的离子方程式_____________________;在一定条件下1g①的单质在足量③的单质中完全燃烧生成液态物质时,放出的热量为a kJ;请写出此条件下表示①的单质燃烧热的热化学方程式
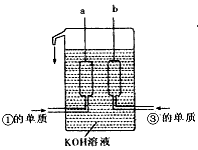
______________________; ①、③两种元素的单质已被应用于字宙飞船的燃料电池中,如图所示,两个电极均由多孔性碳构成,通入的两种单质由孔隙逸出并在电极表面放电。
请回答:b是电池的_________极;a电极上的电极反应式是__________________________。
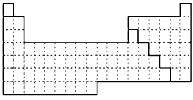
(1)
(2)A.NaOH>Mg(OH)2;B.HF>HCl;C.N2;D.b;cd
(3)Al2O3+2OH-==2AlO2-+H2O;H2(g)+1/2O2(g)==H2O(l);△H=-2akJ/mol;正极;
H2-2e-+2OH-==2H2O
