问题
问答题
32.64g铜和一定浓度的硝酸反应,铜完全溶解产生NO和NO2的混合气体在标准状况下的体积为11.2L,求生成的NO和NO2的物质的量.
答案
32.64g铜的物质的量为
=0.51mol,在反应中失去的电子的物质的量为2×0.51mol=1.02mol,32.64g 64g/mol
11.2L混合气体的物质的量为
=0.5mol,11.2L 22.4L/mol
设混合气体中含有xmolNO,ymolNO2,
则x+y=0.5(质量守恒) 3x+y=1.02(电子守恒)
解之得:x=0.26 y=0.24
答:生成的NO和NO2的物质的量分别为0.26mol、0.24mol.

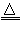 N2↑+4H2O+Cl2↑+2O2↑+Q(化学反应放出能量)下列对此反应的叙述中错误的是 [ ]
N2↑+4H2O+Cl2↑+2O2↑+Q(化学反应放出能量)下列对此反应的叙述中错误的是 [ ]