元素M的离子与NH4+所含电子数和质子数均相同,则M的原子结构示意图为______。
(2)硫酸铝溶液与过量氨水反应的离子方程式为______。
(3)能证明Na2SO3溶液中存在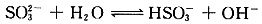 水解平衡的事实是______(填序号)。
水解平衡的事实是______(填序号)。
A.滴入酚酞溶液变红,再加入H2SO4溶液后红色退去
B.滴入酚酞溶液变红,再加入氯水后红色退去
C.滴入酚酞溶液变红,再加入BaCl2溶液后产生沉淀且红色退去
(4)元素X、Y在周期表中位于同一主族,化合物Cu2X和Cu2Y可发生如下转化(其中D是纤维素水解的最终产物):

①非金属性X______Y(填“>”或“<”)。
②Cu2Y与过量浓硝酸反应有红棕色气体生成,化学方程式为______。
(5)在恒容绝热(不与外界交换能量)条件下进行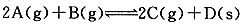 反应,按下表数据投料,反应达到平衡状态,测得体系压强升高。简述该反应的平衡常数与温度的变化关系:()。
反应,按下表数据投料,反应达到平衡状态,测得体系压强升高。简述该反应的平衡常数与温度的变化关系:()。
| 物质 | A | B | C | D |
| 起始投料/mol | 2 | 1 | 2 | 0 |
参考答案:
(1)
(2)
(3)C
(4)①< ②
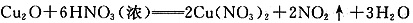
(5)平衡常数随温度的升高而变小(或其他合理答案)
解析:
本题主要涉及元素化合物知识。
(1)由题意,元素M与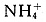 所含的电子数和质子数均相同,则M为Na原子。
所含的电子数和质子数均相同,则M为Na原子。
(2)氨水是弱电解质,用化学式表示。
(3)氯水具有漂白作用,不能证明平衡移动了;加入BaCl2溶液后,平衡发生移动。
(4)根据氧化的顺序,可知非金属性X<Y。
(5)由表可知,起始时反应向正反应方向进行,恒容绝热条件下,体系压强增大,说明正反应为放热反应,可知平衡数随温度的升高而减小。
