问题
问答题
现有FeCl3、AlCl3的混合溶液200mL,逐滴加入NaOH溶液,生成沉淀的物质的量随加入的NaOH的物质的量的关系如图,请计算出:
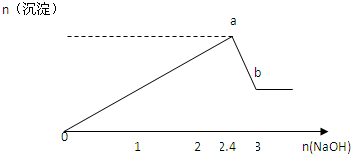
(1)FeCl3、AlCl3的物质的量浓度各为多少?
(2)a点沉淀的质量.
答案
(1)设n(Al3+)=n(Al(OH)3)=x,则
由Al(OH)3+OH-═AlO2-+2H2O
1 1
x (3-2.4)mol
=1 1
,解得x=0.6mol,x (3-2.4)mol
设n(Fe3+)=y,则
Al3++3OH-═Al(OH)3↓
0.6mol 1.8mol
Fe3++3OH-═Fe(OH)3↓
1 3
y (2.4-1.8)mol
=1 3
,解得y=0.2mol,y (2.4-1.8)mol
则c(FeCl3)=
=1mol/L,c(AlCl3)=0.2mol 0.2L
=3mol/L,0.6mol 0.2L
答:FeCl3、AlCl3的物质的量浓度各为1mol/L、3mol/L;
(2)由Fe3++3OH-═Fe(OH)3↓、Al3++3OH-═Al(OH)3↓可知,a点的沉淀为Fe(OH)3和Al(OH)3,
则a点沉淀的质量为0.2mol×107g/mol+0.6mol×78g/mol=68.2g,
答:a点沉淀的质量为68.2g.
