问题
问答题
在Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O反应中, △ .
(1)请用双线桥法标出电子得失情况,______
(2)若有0.1mol Cu发生了反应,则转移的电子个数为______;若有0.1mol电子发生了转移,则所生成的SO2气体在标准状况下的体积为______.
答案
(1)该氧化还原反应中,得电子的元素是硫,化合价降低2价,失电子的元素是铜,化合价升高2价,所以转移电子2mol,如下所示:
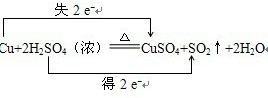
,故答案为:

;
(2)反应Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O中,消耗1mol铜,转移的电子是2mol,当有0.1molCu发生了反应,则转移电子0.2mol,个数为0.2mol×6.02×1023mol-1=1.202×1022,反应中转移的电子是2mol时,生成的SO2气体物质的量为1mol,当转移0.1mol电子时,则生成二氧化硫的物质的量是0.05mol,体积是:0.05mol×22.4L/mol=1.12L. △ .
故答案为:1.202×1022;1.12L.
