某研究性小组借助A-D的仪器装置完成有关实验
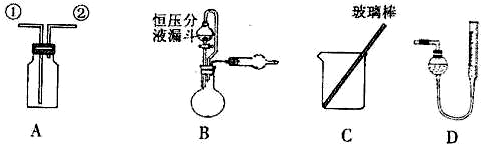
【实验一】收集NO气体.
(1)用装置A收集NO气体,正确的操作上______(填序号).
a.从①口进气,用排水法集气 b.从①口进气,用排气法集气
c.从②口进气,用排水法集气 d..从②口进气,用排气法集气
【实验二】为了探究镀锌薄铁板上的锌的质量分数ωZn和镀层厚度,查询得知锌易溶于碱:Zn+2NaOH=Na2ZnO3+H2↑据此,截取面积为S的双面镀锌薄铁板试样,剪碎、称得质量为m1g.用固体烧碱和水作试剂,拟出下列实验方案并进行相关实验.
方案甲:通过测量试样与碱反应生成的氢气体积来实现探究木目标.
(2)选用B和______(填仪器标号)两个装置进行实验.
(3)测得充分反应后生成氢气的体积为VL(标准状况),ω(Zn)═______.
(4)计算镀层厚度,还需要检索的一个物理量是______.
(5)若装置B中的恒压分液漏斗改为普通分液漏斗,测量结果将______(填“偏大”、“偏小”或“无影响”).
方案乙:通过称量试样与碱反应前后的质量实现探究目标.选用仪器C做实验,试样经充分反应,滤出不溶物、洗涤、烘干,称得其质量为m2g.
(6)ω(Zn)=______.
方案丙:通过称量试样与碱反应前后仪器、试样和试剂的总质量(其差值即为H2的质量)实现探究目标.实验同样使用仪器C.
(7)从实验误差角度分析,方案丙______方案乙(填“优于”、“劣于”或“等同于”).
(1)NO遇空气立即被氧化,故不能用排空气法收集,只能用排水法收集.排水时应用短进长出,故答案为:C;
(2)方案甲:Zn和Fe中只有Zn可以与NaOH产生气体,通过排水收集气体,依据反应方程式即可算出Zn的质量分数.所以需要的装置有测H2的体积的D装置.故答案为:D;
(3)Zn与H2之间量为1:1,则n(Zn)=
,w (Zn)=V 22.4mol
=m(Zn) m1
.故答案为:65V 22.4m1
(或65V 22.4m1
等其他合理答案);2.9V m1
(4)有了Zn的质量,如果有密度,则可以求出Zn的体积,再由Zn的截面积,即可求出Zn的高度(厚度).故答案为:金属锌的密度(或其他合理答案);
(5)恒压式分液漏斗产生的气体有部分残留在分液漏斗上方,故排气时收集少了,所以用普通漏斗时收集的H2多一些,则计算出的Zn的量偏大.故答案为:偏大;
(6)减少的质量即为Zn的质量.减少的质量为m1g-m2g,ω(Zn)=
,故答案为:m1-m2 m1
(或其他合理答案)m1-m2 m1
(7)丙方案根据H2的质量差值,显然误差大,因为产生的H2质量很小,计算偏差大.故答案为:劣于.
