能源短缺是人类社会面临的重大问题。甲醇是一种可再生能源,具有广泛的开发和应用前景。
(1)工业上一般采用下列两种反应合成甲醇:
反应I: CO(g) + 2H2(g)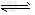 CH3OH(g) ΔH1
CH3OH(g) ΔH1
反应II:CO2(g) + 3H2(g)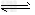 CH3OH(g) + H2O(g) ΔH2
CH3OH(g) + H2O(g) ΔH2
①在以上制备甲醇的两个反应中:反应I优于反应II,原因为___________。
②下表所列数据是反应I在不同温度下的化学平衡常数(K)。

I、在一密闭容器中发生反应Ⅰ并达到平衡后,保持其他条件不变,对容器升温,此反应的化学反应平衡应__________移动(填“正向”、“逆向”、“不”) 。
II、某温度下,将1mol CO和4mol H2充入2L的密闭容器中,充分反应达到平衡后,测得c(CO)= 0.1 mol/L,则CO的转化率为___________,此时的温度______________250℃(填“>”、“<”、“=”)
(2)已知在常温常压下:
① 2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(g) ΔH = -1275.6 kJ/mol
② 2CO (g)+ O2(g) = 2CO2(g) ΔH = -566.0 kJ/mol
③ H2O(g) = H2O(l) ΔH = -44.0 kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:__________________
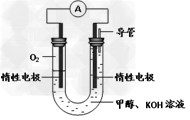
(3)某同学依据甲醇燃烧的反应原理,设计如图所示的电池装置,工作一段时间后,测得溶液的pH将____________(填“升高”、“降低”、“不变”),该燃料电池负极反应的离子方程式为:___________________。
(1)①反应I符合“原子经济性”的原则即原子利用率为100%
②I:逆向 ; II:80% ; <
(2)CH3OH(l)+ O2(g) = CO(g) + 2H2O(l) ΔH=﹣442.8 kJ∕mol
(3)降低 ; CH3OH-6e-+8OH-=CO32- +6H2O
