已知X是一种酸式盐,H是常见金属单质,F、I是常见非金属单质,D为淡黄色固体,E、G都是工业上重要的碱性物质,A物质可做耐火材料.它们有如图所示的转化关系.
试回答下列问题
(1)X的化学式为:______;G的电子式为______.
(2)写出下列反应的化学方程式
①______ ②______.
(3)H与同周期原子序数比其大一的另一种金属组成原电池,H作正极,则负极反应式为______,电解质溶液为______.
(4)H的工业制法可用电解原理,当阳极产生可使湿润的淀粉KI试纸变蓝的气体1.12升(标况)时,阴极生成H______克,有关化学方程式为______.

H是常见金属单质,I是常见非金属单质,根据关系图,可知H+B=A+I,此为点燃条件下置换反应,且为金属置换非金属,A物质可做耐火材料,初步确定为2Mg+CO2=2MgO+C,H为Mg,B为CO2,I为C,所以A为MgO,A由X分解得到,且X为酸式盐,应为碳酸氢镁,B是CO2,C为H2O,二者均能和D反应,D为淡黄色固体,且都生成F,F是常见非金属单质,可知D为过氧化钠,F为氧气.根据关系图,可知E为碳酸钠,G为氢氧化钠.进行验证符合.
故A为MgO,B是CO2,C为H2O,D为过氧化钠,E为碳酸钠,F为氧气,G为氢氧化钠,H为Mg,I为C.
(1)X为碳酸氢镁,化学式为Mg(HCO3)2;G为氢氧化钠,由钠离子与氢氧根离子构成,电子式为
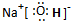
.
故答案为:Mg(HCO3)2;
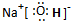
.
(2)①二氧化碳与过氧化钠反应生成碳酸钠与氧气,反应方程式为2Na2O2+2CO2=2Na2CO3+O2.
故答案为:2Na2O2+2CO2=2Na2CO3+O2 .
②水与过氧化钠反应生成氢氧化钠与氢气,反应方程式为2Na2O2+2H2O═4NaOH+O2↑.
故答案为:2Na2O2+2H2O═4NaOH+O2↑.
(3)H为Mg,Mg与Al组成原电池,Mg作正极,则电解质溶液与Al反应,不与Mg反应,电解质溶液为强碱如NaOH溶液,Al为负极,则负极反应式为Al+4OH--3e-=AlO2-+2H2O.
故答案为:Al+4OH--3e-=AlO2-+2H2O;NaOH溶液.
(4)工业上利用电解熔融的氯化镁生成镁,电解总反应式为MgCl2(熔融)
Mg+Cl2↑,阳极产生的氯气为 电解 .
=0.05mol,由电解总反应式可知,生成Mg0.05mol,所以生成Mg的质量为0.05mol×24g/mol=1.2g.1.12L 22.4L/mol
故答案为:1.2;MgCl2(熔融)
Mg+Cl2↑. 电解 .
