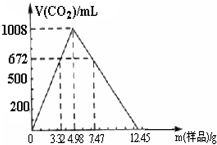
自然界存在某天然碱(纯净物)的化学组成可表示为aNa2CO3•bNaHCO3•cH2O(a、b、c 为正整数).现称取不同质量的天然碱样品,溶于水后,分别逐滴加入相同浓度的盐酸溶液30.0ml,产生CO2 的体积(标准状况)如图所示.
(1)若用2.49g样品进行同样的实验时,产生CO2______mL(标准状况).
(2)另取3.32g天然碱样品于3000C加热分解至完全(3000C 时Na2CO3 不分解)产生CO2 112ml(标准状况)和水0.450g,试通过计算确定该天然碱的化学式.
(3)实验所用盐酸的物质的量浓度是多少?
(4)若在上述某次实验中,收集到336ml(标准状况)的气体,该此实验中称取天然碱样品的质量可能是多少?
解析:题中图示表示将30mL盐酸逐滴加入样品溶液中,所加样品质量与生成CO2的体积(标准状况)的关系.
(1)m(样品)≤4.98g时,样品质量与CO2体积成正比.设2.49g样品反应生成CO2的体积为V,则
=2.49g V
,V=504mL,故答案为:504;3.32g 672ml
(2)3.32g样品中,n(NaHCO3)=2n(CO2)=2×
=0.01mol,0.112L 22.4L/mol
n(H2O)=
=0.02mol.0.45g-0.005mol×18g/mol 18g/mol
由碳元素守恒得:
n(Na2CO3)=
-0.01mol=0.02mol,则n(Na2CO3):n(NaHCO3):n(H2O)=0.02mol:0.01mol:0.02mol=2:1:2.0.672L 22.4L/mol
故该天然碱的组成为:2Na2CO3・NaHCO3・2H2O.
答:该天然碱的组成为:2Na2CO3・NaHCO3・2H2O.
(3)当4.98g≤m(样品)≤12.45g时,30mL盐酸全部参加反应.其中m(样品)=4.98g时,样品中Na2CO3、NaHCO3都恰好生成CO2;m(样品)=12.45g时,样品中Na2CO3恰好生成NaHCO3.任一情形用于计算盐酸浓度都很方便.
样品质量为4.98g时,反应式为:
2Na2CO3・NaHCO3・2H2O+5HCl=5NaCl+3CO2↑+5H2O
由以上可知,消耗n(HCl)=
×5=0.075mol,c(HCl)=4.98g 332g/mol
=2.5mol/L,0.075mol 0.03L
答:实验所用盐酸的物质的量浓度是2.5mol/L.
(4)收集到336ml气体时,可能存在两种情况:①盐酸过量,②天然碱过量,
①盐酸过量时,设天然碱的质量为x,
则
=x 336ml
,x=1.16g;3.32g 672ml
②天然碱过量时,设需要ymol天然碱,
则含有2ymolNa2CO3,ymolNaHCO3,发生反应有:
Na2CO3+HCl=NaHCO3+NaCl
NaHCO3+HCl=CO2↑+NaCl+H2O
则:2y+
=0.03L×2.5mol/L0.336L 22.4L/mol
y=0.03mol,
则m(2Na2CO3••NaHCO3•2H2O)=0.03mol×332g/mol=9.96g.
答:盐酸过量时1.66克; 天然碱过量时9.96克
