自然界存在着一种白云石的矿石,其化学式是xCaCO3•yMgCO3.以它为原料,可制取耐火材料等.
(1)称取27.6g白云石,加热到质量不再变化,可以生成耐火材料MgO多少mol?(用x、y的代数式表示)
(2)若在上述反应中,收集到CO26.72L(标准状况下),试写出白云石的化学式(取x、y的最小正整数比).
(3)若称取白云石mg,研碎后与过量炭粉混合,放在特定仪器中隔绝空气强热一段时间后,测得白云石分解率为a,生成一氧化碳的体积为VL(标准状况),试计算,V=______(用m、a代数式表示)
(已知CaO+3C
CaC2+CO高温
2MgO+5C
Mg2C3+2CO高温
CO2+C
2CO)高温
请在图中画出V和a的关系图.
(1)生成耐火材料MgO的物质的量为n(MgO)=n(Mg)=
×y=27.6g (100x+84y)g/mol
mol,27.6y 100x+84y
答:生成耐火材料MgO的物质的量为
mol;27.6y 100x+84y
(2)根据题意,白云石受热分解的化学方程式为:
二氧化碳的质量为
×44g/mol=1.32g,6.72L 22.4L/mol
xCaCO3•yMgCO3
xCaO+yMgO+(x+y)CO2↑ 高温 .
100x+84y 44(x+y)
2.76g 1.32g
所以
=100x+84y 2.76g
,44(x+y) 1.32g
解得 x:y=1:1,
因此白云石的化学式为CaCO3•MgCO3,
答:白云石的化学式为CaCO3•MgCO3;
(3)由CaCO3•MgCO3
CaO+MgO+2CO2↑, 高温 .
CaO+3C
CaC2+CO高温
2MgO+5C
Mg2C3+2CO高温
CO2+C
2CO,则可知 高温 .
CaO~CO MgO~CO CO2~2CO
即存在CaCO3•MgCO3~6CO
184 6×28
mg×a
×28g/mol=1.25VgVL 22.4L/mol
所以
=184 mag
,6×28 1.25Vg
解得V=0.73ma,
故答案为:0.73ma;
由V=0.73ma可知,V和a的关系在坐标图上为斜率为2.02,的正比例图象关系,
答:V和a的关系图为
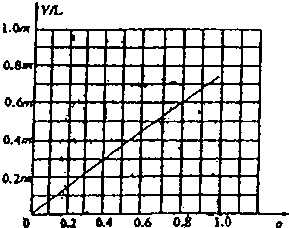
.
