问题
填空题
请将氧化还原反应:2Fe3++2I- ==2Fe2++I2设计成带盐桥原电池。试剂:FeCl3溶液,KI溶液;其它用品任选。请回答下列问题。
(1)请画出设计的原电池装置图,并标出电极材料,电极名称及电解质溶液。

(2)发生还原反应的电极为电池的_______极,其电极反应式为_______________ 。
(3)反应达到平衡时,外电路导线中________(填“有”或“无”)电流通过。
(4)平衡后向FeCl3溶液中加入少量FeCl2固体,当固体全部溶解后,则此时该溶液中电极变为________(填“正”或“负”)极。
(5)请设计简单实验,证明溶液中同时存在Fe3+ 、Fe2+______________________。
答案
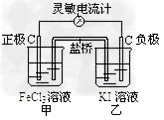
(1)
(2)正;Fe3++e-=Fe2+
(3)无
(4)负
(5)取少量待检液于试管中,加入硫氰化钾,显红色,说明有Fe3+;另取少量待检液于试管中,加入酸性高锰酸钾溶液,若溶液退色,则有Fe2+。
