问题
选择题
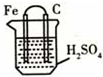
下列关于图所示装置的叙述,不正确的是( )
A.铁是负极,铁失去电子形成Fe2+进入溶液
B.铁片质量逐渐减少,碳棒上有气泡产生
C.电流由铁片经导线沿外电路流向碳棒
D.该装置总的化学反应为Fe+H2SO4═FeSO4+H2↑
答案
在该原电池中,自发的氧化还原反应是金属铁和硫酸之间的反应,金属铁为负极,碳棒为正极.
A、在该原电池中,金属铁为负极,失电子形成亚铁离子进入电解质,故A正确;
B、在该原电池中,金属铁为负极,负极金属质量减轻,正极碳棒上放氢气,故B正确;
C、在该原电池中,电子由铁片经导线沿外电路流向碳棒,电流流向和电子流向相反,故C错误;
D、原电池的总反应是金属铁和硫酸之间的反应,即Fe+H2SO4═FeSO4+H2↑,故D正确.
故选C.
