卤水(提取食盐后的母液)含有MgCl2、NaCl、MgSO4、KCl.从卤水中提取KCl固体,采用下列方法:
(1)将卤水加热到60℃以上蒸发水分就逐渐析出晶体A,滤出晶体得到母液R,根据下图所示溶解度曲线,晶体A中主要含有______和______,理由是______.
(2)将母液R降温(降到30℃以下)析出晶体B,则晶体B主要含有______和______,理由是______.
(3)将析出的晶体B,用一定量的冷水洗涤,就可以得到较纯的KCl固体,理由是______.
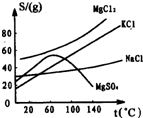
(1)观察溶解度图象,当温度大于60℃,随着温度的升高,MgSO4的溶解度反而下降,NaCl的溶解度一直比较低.所以这两种物质就会结晶析出,故答案为:NaCl,MgSO4;温度高于60℃时这两种物质的溶解度较小.
(2)降温时析出晶体,说明该晶体溶解度随温度的降低而降低;从图象可以看出,MgCl2和KCl随着温度的降低而下降,故答案为:MgCl2,KCl;由于温度下降,这两种物质溶解度也随之下降.
(3)降温时析出晶体,说明该晶体溶解度随温度的降低而降低;从图象可以看出,在温度较低时,MgCl2的溶解度大于KCl的溶解度;所以冷水洗涤时较纯的KCl固体就会析出.故答案为:低于30℃时,MgCl2的溶解度大于KCl的溶解度,所以,用少量冷水淋洗析出的晶体,就得到较纯的KCl晶体.
