如图所示3套实验装置,分别回答下列问题.
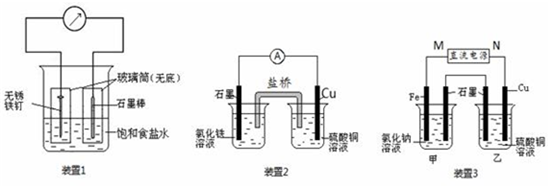
(1)装置1为铁的吸氧腐蚀实验.向插入碳棒的玻璃筒内滴入酚酞溶液,可观察到碳棒附近的溶液变红,该电极反应为______.
(2)装置2中的石墨是______极(填“正”或“负”),该装置发生的总反应的离子方程式为______.
(3)装置3中甲烧杯盛放100mL 0.2mol/L的NaCl溶液,乙烧杯盛放100mL 0.5mol/L的CuSO4溶液.反应一段时间后,停止通电.向甲烧杯中滴入几滴酚酞,观察到石墨电极附近首先变红.
①电源的M端为______极;甲烧杯中铁电极的电极反应为______.
②乙烧杯中电解反应的离子方程式为______.
③停止电解,取出Cu电极,洗涤、干燥、称量、电极增重0.64g,甲烧杯中产生的气体标准状况下体积为______mL.
(1)装置1为铁的吸氧腐蚀实验,发生电化学腐蚀,铁为负极,碳为正极,观察到碳棒附近的溶液变红,说明在碳极上氧气得电子生成OH-离子,反应的电极反应式为
O2+4e-+2H2O═4OH-,故答案为:O2+4e-+2H2O═4OH-;
(2)装置2为原电池,负极为Cu,电极反应为:Cu-2e-═Cu2+,正极为石墨,电极反应为2Fe+2e-═2Fe2+,反应的总方程式为2Fe3++Cu═2Fe2++Cu2+,
故答案为:正;2Fe3++Cu═2Fe2++Cu2+;
(3)①反应一段时间后,停止通电.向甲烧杯中滴入几滴酚酞,观察到石墨电极附近首先变红,说明在石墨电极上生成OH-离子,电极反应为:2H2O+2e-═2OH-+H2↑,
发生还原反应,为电解池的阴极,连接电源的负极,即M端为正极,N端为负极,阳极反应为Fe-2e-═Fe2+,故答案为:正;Fe-2e-═Fe2+;
②乙烧杯电解硫酸铜溶液,石墨为阳极,电极反应为4OH--4e-═O2↑+H2O,Cu为阴极,电极反应为Cu2++2e-═Cu,电解的总反应为2Cu2++2H2O
2Cu+O2↑+4H+, 电解 .
故答案为:2Cu2++2H2O
2Cu+O2↑+4H+; 电解 .
③取出Cu电极,洗涤、干燥、称量、电极增重0.64g,则生成Cu的物质的量为
=0.01mol,转移的电子的物质的量为0.01mol×2=0.02mol,0.64g 64g/mol
根据甲烧杯产生气体的电极反应计算生成气体的体积,
2H2O+2e-═2OH-+H2↑,
2mol 22.4L
0.02mol V
V=
=0.224L,即224ml,故答案为:224.22.4L×0.02mol 2mol
