问题
选择题
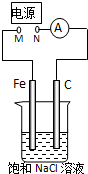
如图所示,将纯Fe棒和石墨棒插入1L 饱和NaCl溶液中.下列说法正确的是( )
A.去掉电源,将M、N用导线直接相连,则Fe棒上产生气泡
B.M连接电源正极,N连接电源负极,则Fe棒被保护不会溶解
C.M连接电源负极,N连接电源正极,当两极产生气体总量为 22.4mL(标准状况)时,则生成0.001mol NaOH
D.M连接电源负极,N连接电源正极,如果把烧杯中的溶液换成1L CuSO4溶液,反应一段时间后,烧杯中产生蓝色沉淀
答案
A.去掉电源,该装置是原电池,铁发生吸氧腐蚀,铁棒上的电极反应式为:Fe-2e-=Fe2+,故A错误;
B.M连接电源正极,N连接负极,则该装置是电解池,铁作阳极,石墨作阴极,铁棒上的电极反应式为:Fe-2e-=Fe2+,所以铁被腐蚀,故B错误;
C.M连接电源负极,N连接正极,该装置是电解池,铁作阴极,石墨作阳极,电池反应式为:
2NaCl+2H2O
(Cl2 ↑+H2↑)+2NaOH 电解 .
44.8L 2mol
0.0224L 0.001mol
所以当两极产生气体总量为 22.4mL(标准状况)时,则生成0.001mol NaOH,故C正确;
D.M连接电源负极,N连接正极,该装置是电解池,铁作阴极,石墨作阳极,电池反应式为:2CuSO4+2H2O
2H2SO4+O2↑+2Cu,溶液呈酸性,所以没有蓝色沉淀生成,故D错误; 电解 .
故选C.
