问题
选择题
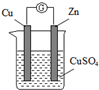
如图甲把锌片和铜片用导线相连后插入硫酸铜溶液构成原电池.某实验兴趣小组做完实验后,在读书卡上的记录如图=2\*ZODIAC1 乙所示,则卡片上的描述合理的是( )
①Cu为正极,Zn为负极;
②Zn质量减少,Cu质量不变;
③SO42-向Cu极移动;
④电子流向是:由Zn经导线流入Cu片;
⑤溶液中Cu2+离子和SO42-离子浓度都减小;
⑥正极反应式:Cu2++2e-=Cu.
A.①②④
B.①④⑥
C.①⑤⑥
D.④⑤⑥
答案
①该原电池中锌失电子变成锌离子进入溶液,所以锌作负极,铜作正极.故正确.
②锌失电子变成锌离子进入溶液,锌片逐渐溶解,所以锌片质量减少,溶液中铜离子得电子生成铜附着在铜极上,所以铜片质量增加,故错误.
③锌失电子通过导线流向铜,所以铜片上有大量电子,根据异性电荷相吸,所以溶液中氢离子向Cu极移动,硫酸根离子向锌极移动,故错误.
④锌失电子通过导线流向铜,所以电子流向为由Zn经导线流入Cu片,故正确.
⑤溶液中铜离子得电子生成铜析出,硫酸根离子不参加反应,所以铜离子浓度减小,硫酸根离子浓度不变,故错误.
⑥铜作正极,正极上铜离子得电子生成铜,电极反应式为Cu2++2e-=Cu,故正确.
故选B.
