问题
选择题
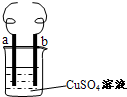
用铁丝(电极a)、铜丝(电极b)和CuSO4溶液可以构成原电池或电解池,如图所示.则下列说法正确的是( )
A.构成原电池时b极反应为:Cu-2e-=Cu2+
B.构成电解池时a极质量一定减少
C.构成电解池时b 极质量可能减少也可能增加
D.构成的原电池或电解池工作后就可能产生大量气体
答案
A、构成原电池时,较不活泼的金属铜作正极,正极上溶液中铜离子得电子生成铜单质而析出,电极反应式为
Cu2++2e-=Cu,故A错误.
B、构成电解池时,连接电源正极的电极为阳极,阳极上金属电极失电子发生氧化反应,如a连接电源负极,则质量增加,故B错误.
C、构成电解池时,连接电源正极的电极为阳极,阳极上金属电极失电子发生氧化反应,连接电源负极的电极为阴极,阴极上铜离子得电子发生还原反应;如果b为阳极,电解池工作时,铜失电子生成铜离子进入溶液导致电极质量减少,如果b为阴极,溶液中铜离子得电子生成铜单质而析出附着在b电极上,导致电极质量增加,故C正确.
D、构成原电池时,正极上铜离子得电子而析出;构成电解池时,阴极上溶液中铜离子得电子而析出,所以无论是原电池还是电解池都没有气体生成,故D错误.
故选D.
