该图装置中,A为铅蓄电池,C1、C2为石墨电极,B烧杯中是浓度均为0.1mol/L的H2SO3和KI的混合溶液100mL.下列说法正确的是( )
A.铅蓄电池工作一段时间后,A中溶液的PH变小
B.当B烧杯中I-的浓度降为0.05mol/L时,A中消耗的H2SO4的物质的量为0.025mol
C.当C1、C2两极均开始产生气体时,至少已有3.6×1022个电子从电路中流过
D.铅蓄电池工作时,负极电极反应式为:PbO2-2e -+H2SO3=PbSO4+2H2O+SO42-
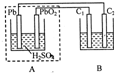
装置中左边装置是原电池,右边装置连接外加电源属于电解池.
A、铅蓄电池放电时,正极上二氧化铅得电子和硫酸反应生成硫酸铅和水,导致溶液的PH值增大,故A错误.
B、当B烧杯中I-的浓度降为0.05mol/L时,电解质溶液中亚硫酸根离子全部为氧化生成硫酸根离子,生成硫酸根离子的物质的量是0.1mol/L×0.1L=0.01mol,转移电子数是0.01mol×2=0.02mol,消耗碘离子的物质的量是0.05mol/L×0.1L=0.005mol,转移电子是0.005mol,所以总共转移电子0.025mol,A中正极上发生的电极反应式为
PbO2+2H2SO4+2e-=PbSO4+2H2O
2mol 2mol
0.025mol 0.025mol
所以A中消耗的H2SO4的物质的量为0.025mol,故B正确.
C、当C1、C2两极均开始产生气体时,碘离子放电完全,根据碘离子的物质的量计算通过的电子个数,碘离子的物质的量=0.1mol/L×0.1L=0.01mol,
2I--2e-=I2
2mol 2NA
0.01mol 0.01NA
所以至少已有6.02×1021个电子从电路中流过,故C错误.
D、铅蓄电池放电时,负极上铅失去电子和硫酸根离子反应生成硫酸铅,电极反应式为 Pb+SO42--2e-=PbSO4,故D错误.
故选B.
