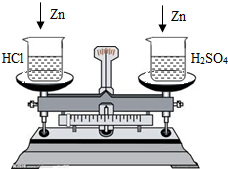
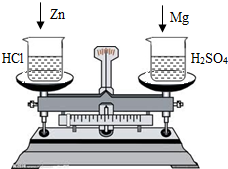
问题
选择题
下列叙述正确的是( )
A.用石墨电极电解MgCl2饱和溶液的总反应为:Mg2++2Cl-
Mg+Cl2↑通电
B.精炼铜过程中阴极增重3.2g时,电路中转移电子数大于0.1NA
C.氢氧酸性燃料电池放电时,正极反应为:O2+4e-+4H+=2H2O
D.铅蓄电池在放电过程中,负极质量减小,正极质量增加
答案
A、用石墨电极电解MgCl2饱和溶液,阳极上氯离子放电,阴极上氢离子放电,所以实际上相当于电解水,电解反应式为2H2O
2H2↑+O2↑,故A错误; 电解 .
B、精炼铜时,阴极上铜离子得电子生成铜单质,1mol铜离子得到2mol电子生成铜单质,生成3.2g铜需要转移电子0.1NA,故B错误;
C、氢氧酸性燃料电池放电时,正极上氧气得电子和氢离子反应生成水,电极反应式为O2+4e-+4H+=2H2O,故C正确;
D、铅蓄电池在放电过程中,正、负极质量都减少,故D错误.
故选C.