问题
选择题
根据如图,下列判断中正确的是( )
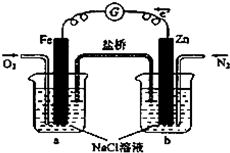
A.向烧杯a中加入少量K3[Fe(CN)6]溶液,有蓝色沉淀生成
B.烧杯b中发生反应为2Zn-4e-=2Zn2+
C.电子从Zn极流出,流入Fe极,经盐桥回到Zn极
D.烧杯a中发生反应O2+4H++4e-=2H2O,溶液pH降低
答案
A.烧杯a中发生的氧气得到电子生成氢氧根离子的反应,电极反应为:O2+2H2O+4e-=4OH-,铁不被氧化,则向烧杯a中加入少量K3[Fe(CN)6]溶液,没有蓝色沉淀生成,故A错误;
B.烧杯中Zn为负极,则b中发生的反应为Zn-2e-=Zn2+,故B正确;
C.电子不能流经溶液,溶液中由离子的定向移动导电,故C错误;
D.a中Fe为正极,发生O2+2H2O+4e-=4OH-,碱性增强,pH增大,故D错误.
故选B.
