认真观察如图装置,试回答下列问题:
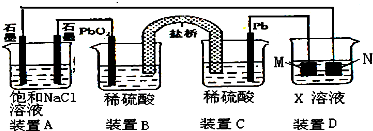
(1)连接装置B、C之间的U形管中装填有含有琼脂的KCl饱和溶液,电池工作时,对盐桥中的K+、Cl-的移动方向为______.装置B中PbO2上发生的电极反应式为______.
(2)装置A中总反应的离子方程式为______.
(3)若装置D的目的是在某镀件上镀银,则X为______,电极板N的材料为______.
(4)当装置D中镀件质量增加21.6g时,装置A中产生的气体体积为______L(标准状况下,不考虑气体的溶解).
(1)B和C装置形成原电池,铅作负极,二氧化铅作正极,原电池放电时,盐桥中阳离子向正极移动,阴离子向负极移动,所以K+向B装置方向移动,Cl-向C装置方向移动,正极上二氧化铅得电子和硫酸根离子反应生成硫酸铅,电极反应式为:PbO2+2e-+4H++SO42-═PbSO4+2H2O
故答案为:K+向B装置方向移动,Cl-向C装置方向移动;PbO2+2e-+4H++SO42-═PbSO4+2H2O;
(2)A连接电源,则A是电解池,左边石墨作阴极,右边石墨作阳极,阳极上氯离子放电,阴极上氢离子放电,所以电池反应式为:2Cl-+2H2O
Cl2↑+H2↑+2OH-,故答案为:2Cl-+2H2O电解 .
Cl2↑+H2↑+2OH-;电解 .
(3)镀时,镀层作阳极,镀件作阴极,电解质溶液中阳离子和镀层金属相同,若装置D的目的是在某镀件上镀银,则X为硝酸银溶液,N作阳极,应该是银,
故答案为:AgNO3溶液;Ag;
(4)当装置D中镀件质量增加21.6g时,转移电子的物质的量=
×1=0.2mol,装置A中电池反应式为:2Cl-+2H2O21.6g 108g/mol
Cl2↑+H2↑+2OH-,根据转移电子相等知,生成气体体积=电解 .
×2×22.4L/mol=4.48L,故答案为:4.48.0.2mol 2
