(10分)铬是人体必需元素,如含量不足会影响糖类和脂类的代谢,过高则会引起急性中毒。有关含铬化合物的相互转化关系如下
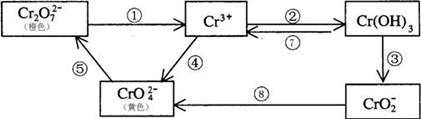
回答下列问题:
(1)上述反应中需用氧化剂的是 (填编号)。
(2)工业上处理含Cr2O72-的废水时,一般将剧毒的Cr2O72-转化为Cr3+,以碳为阴极,铁作阳极,电解处理含NaCl、Cr2O72-的酸性废水。写出电极反应和溶液中进行的反应的离子方程式:
阳极 阴极
溶液中
(3)反应⑤是可逆反应,在Na2CrO4溶液中加入稀硫酸,溶液由黄色逐渐变成橙色,写出该反应的离子方程式 。
(1) 4 8
(2 )2H++2e-=H2↑ Fe-2e-=Fe2+ Cr2O72- + 6Fe2+ + 14H+ = 2Cr3+ +6Fe3++7H2O
(3)2CrO42-+2H+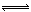 Cr2O72-+H2O
Cr2O72-+H2O
本题考查了氧化还原反应、离子反应及电化学的相关知识;
(1)根据铬的化合价可知,化合价升高的反应必然是由外界提供氧化剂
(2)阳极铁要失电子 Fe-2e-=Fe2+,再根据离子的放电顺序知道H+在阴极放电2H++2e-=H2↑ ;
Fe2+的产生提供了还原剂,被Cr2O72-氧化:Cr2O72- + 6Fe2+ + 14H+ = 2Cr3+ +6Fe3++7H2O
(3)主要考查离子方程式的书写与配平
