(19分)N2O5是一种新型硝化剂,其性质和制备受到人们的关注。
(1)N2O5与苯发生硝化反应生成的硝基苯的结构简式是______________。
(2)一定温度下,在恒容密闭容器中N2O5可发生下列反应:2N2O5(g) 4NO2(g)+O2(g);ΔH>0
4NO2(g)+O2(g);ΔH>0
①反应达到平衡后,若再通入一定量氮气,则N2O5的转化率将______(填“增大”、“减小”、“不变”)。
②下表为反应在T1温度下的部分实验数据:
| t/s | 0 | 500 | 1000 |
| c(N2O5)/mol·L-1 | 5.00 | 3.52 | 2.48 |
③在T2温度下,反应1000 s时测得NO2的浓度为4.98 mol·L-1,则T2________T1。(填>、<或=)
(3)如右图所示装置可用于制备N2O5,则N2O5在电解池的______区生成,其电极反应式为_______。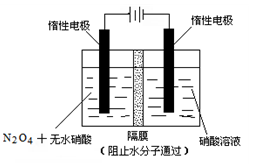
(1)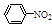 ;(3分)(2)①不变(3分) ②0.00296 mol·L-1·s-1(3分)
;(3分)(2)①不变(3分) ②0.00296 mol·L-1·s-1(3分)
③<(3分)(3)阳极(3分) N2O4+2HNO3-2e—=2N2O5+2H+ (4分)
(1)硝基苯中还有-NO2官能团,结构简式为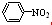 。
。
(2)①通入氮气,但物质的浓度是不变的,所以平衡不移动,转化率不变。
②500s时,消耗N2O5的浓度是1.48mol/L,所以分解速率是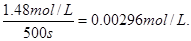
③NO2是4.98mol/L,则消耗N2O5是2.49mol/L,剩余N2O5是2.51mol/L,而温度为T1时是2.48mol/L,这说明温度为T1时反应速率快,所以T1大于T2。
(3)N2O5中氮元素的化合价是+5价,而硝酸中氮元素也是+5价。因此应该在左侧生成N2O5,即在阳极区域生成,方程式为 N2O4+2HNO3-2e—=2N2O5+2H+。
