问题
选择题
读图甲和图乙,D地此时是2008年12月21 的正午,此时一艘轮船从A地出发,航行6天后到达B地,然后又继续航行10天,到达目的地C地(32°N)。回答1—4题。
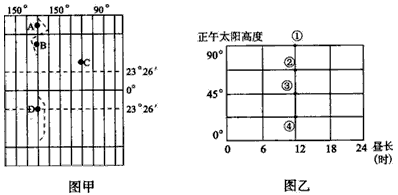
1、轮船出发的当天,下列叙述正确的是[ ]
A、昼长由长到短的排序A>E>C>D
B、太阳高度角由大到小的排序是A>B>C>D
C、此时北半球大陆等温线向南突出
D、此时C地受副热带高压控制
2、轮船到达C地时,该地的时间为[ ]
A、2009年1月6日16时
B、2009年1月5日8时
C、2009年1月5日16时
D、2009年1月6日8时
3、读图乙,当地球公转处于远日点附近时,赤道上的点是[ ]
A、①
B、②
C、③
D、④
4、当C地处于高压的控制下时,图丙中各岛昼长时间由大到小排列正确的是
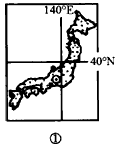
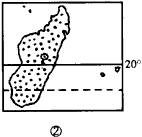
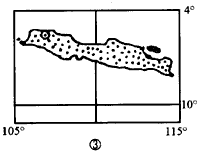
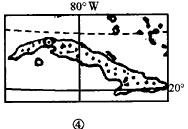
A、②③④①
B、①②③④
C、③④①②
D、①④③②
答案
1、C
2、C
3、B
4、D
