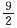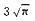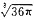问题
选择题
用两根铂丝做电极插入KOH溶液中,再向两个电极上分别通甲烷气和氧气可形成原电池——燃料电池,根据两极反应的实质判断,
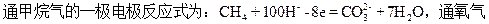
的一极,在下列叙述中正确的是
A.阴极:4H2O+2O2+8e=8OH-
B.正极:4H2O+2O2+8e=8OH-
C.阴极:4OH--4e=2H2O+O2↑
D.正极:4OH--4e=2H2O+O2↑
答案
B
从CH4一极所发生的失电子电极反应式看,通CH4的一极应为原电池的负极,通氧的一极必为原电池的正极,正极应发生得电子的还原反应,且两极得失电子的数目相等,从题给选项看,应选B。