按要求完成下列各小题:
(1)我国古代四大发明之一的黑火药,爆炸时的反应为S+2KNO3+3C=K2S+N2↑+3CO2,该反应中还原剂是 ,氧化剂是 。
(2)制普通玻璃的原料是 ,其中 是制水泥和普通玻璃的共同原料。
(3)用氧化物的形式表示某硅酸盐的组成:K4Al4FeSi6O18(OH)7 .
(4)漂白粉的成分是 ,工业制漂白粉的化学方程式为 漂白粉在空气中保存不当会失效的原因,用化学方程式表示
(5)将23gNa与28g硅同时投入水中,理论上放出H2 g,写出反应中有关的离子方程式 。
(1)C S和KNO3
(2)纯碱、石灰石、石英 石灰石
(3)4K2O·4Al2O3·Fe2O3·12SiO2·7H2O
(4)CaCl2和Ca(ClO)2 2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O
Ca(ClO)2+CO2+H2O=CaCO3+2HClO (未写出2HClO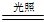 2HCl+O2↑不扣分)
2HCl+O2↑不扣分)
(5)3g 2Na+2H2O=2Na++2OH-+H2 Si+2OH-+H2O=SiO32-+2H2
(1)反应中碳的化合价由0价升至+4价,被氧化,做还原剂;而硫由0价降至—2价、氮由+5价降至0价,故S和KNO3均做氧化剂
(2)制普通玻璃的原料是纯碱、石灰石、石英,制水泥的原料为石灰石、粘土
(3)由原子守恒可知氧化物形式为:4K2O·4Al2O3·Fe2O3·12SiO2·7H2O
(4)工业上将氯气通入石灰乳中制取漂白粉:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,漂白粉的主要成分为CaCl2和Ca(ClO)2的混合物;由于其中的Ca(ClO)2可吸收空气中的CO2而使其失效:Ca(ClO)2+CO2+H2O=CaCO3+2HClO,2HClO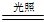 2HCl+O2↑,故漂白粉需要密封保存
2HCl+O2↑,故漂白粉需要密封保存
(5)根据所发生反应知:
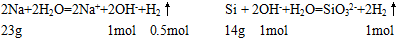
其中钠全部与水反应,生成的碱相对硅来讲不足,最终生成的氢气共1.5mol,质量为3g
