(Ⅰ)某铅蓄电池的正、负极标记被磨损.试用如图装置设计实验,识别出此铅蓄电池的正负极.
(1)若A接E,B接F,而B电极出现______,反应式为______,则说明F为正极;
(2)铅蓄电池工作时(放电),其E所在电极的电极反应式为:______,充电时该极与外加电源的______极相连;
(3)若有0.2mol电子发生转移,则正极消耗的PbO2的物质的量是______;
(Ⅱ)利用甲醇(CH3OH)、氧气组成燃料电池,电解质溶液为碱性,电池工作时,其负极方程式(写离子方程式)为______.
(Ⅲ)一种基于酸性燃料电池原理设计的酒精检测仪,负极上的反应为CH3CH2OH+H2O→CH3COOH+4H++4e-.正极的反应式:______;电池反应的总方程式为:______.
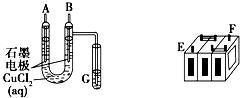
(Ⅰ)(1)与原电池正极相连的为电解池的阳极,所以B为阳极,氯离子在阳极失电子,生成氯气,即在B电极出现黄绿色气体,其电极反应式为2Cl--2e-=Cl2↑,
故答案为:黄绿色气气体产生;2Cl--2e-=Cl2↑;
(2)铅蓄电池工作时负极为Pb失电子,则其电极反应式为:Pb+SO42--2e-=PbSO4;充电时蓄电池的负极与外接电源的负极相连,
故答案为:Pb+SO42--2e-=PbSO4;负;
(3)正极上PbO2→PbSO4,Pb元素从+4降低到+2,转移2个电子,所以若有0.2mol电子发生转移,则正极消耗的PbO2的物质的量是0.1mol,
故答案为:0.1mol;
(II)碱性条件下,负极上甲醇失电子生成碳酸根离子,则其电极反应式为:CH3OH+8OH--6e-=CO32-+6H2O,故答案为:CH3OH+8OH--6e-=CO32-+6H2O;
(III)酸性燃料电池中氧气在正极得电子生成水,其电极反应式为:O2+4H++4e-=2H2O,正极的电极反应式与和负极的电极反应式相加即是总反应,所以电池反应的总方程式为:CH3CH2OH+O2=CH3COOH+H2O,故答案为:O2+4H++4e-=2H2O;CH3CH2OH+O2=CH3COOH+H2O.
