问题
计算题
由铜片、锌片与200 mL硫酸组成的原电池中,若锌片只发生电化学腐蚀,则当在铜片上共放出0.15 mol气体时,H2SO4恰好全部用完。产生这些气体消耗锌多少克?所用硫酸的物质的量浓度是多少?
答案
9.75 g 0.75 mol·L-1
此反应的总反应是
Zn + 2H+ ="=== " Zn2+ + H2↑
65 g 2 mol 1 mol
x y 0.15 mol
x=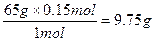 y=
y=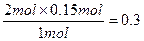 mol
mol
H2SO4的物质的量为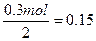 mol
mol
c(H2SO4)=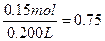 mol·L-1
mol·L-1
