问题
选择题
铅蓄电池作电源时,正极材料是PbO2,负极材料是Pb,内充稀硫酸,两极总反应为Pb+PbO2+2H2SO4 2PbSO4+2H2O,当电压由2.0 V下降到1.85 V,应停止使用,进行充电,则阴极的电极反应式为( )
2PbSO4+2H2O,当电压由2.0 V下降到1.85 V,应停止使用,进行充电,则阴极的电极反应式为( )
A.PbO2+4H++2e- Pb2++2H2O
Pb2++2H2O
B.Pb-2e- Pb2+
Pb2+
C.PbSO4+2e- Pb+SO
Pb+SO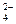
D.PbSO4+2H+-2e- PbO2+4H++SO
PbO2+4H++SO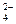
答案
答案:C
+4价的铅(PbO2)有氧化性得到电子,单质铅有还原性,与酸接触失去电子,构成了有较高电位差的两极,电子沿导线流动就构成原电池。放电到一定时候,电位差缩小了(两极都生成PbSO4),欲使两极重新成为PbO2和Pb,即进行充电。阴极发生还原反应:PbSO4+2e- Pb+SO
Pb+SO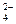 。所以应选C。
。所以应选C。
