问题
选择题
在25℃时,用石墨电极电解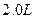 ,
,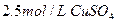 溶液。5min后,在一个石墨电极上有6.4g Cu生成。试回答:
溶液。5min后,在一个石墨电极上有6.4g Cu生成。试回答:
(1)转移电子的物质的量,得到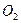 的体积(标准状况),溶液的
的体积(标准状况),溶液的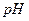 ?
?
2)如用等质量的两块铜片代替石墨作电极,电解后两铜片的质量相差多少?电解液的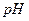 是否变化? (相对原子质量 Cu:64)
是否变化? (相对原子质量 Cu:64)
答案
(1)设转移电子的物质的量为x ,生成氧气的体积为V
2Cu2+ + 4e— = 2Cu
2 4 2
X 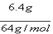 4:x="2:0.1mol " x="0.2mol"
4:x="2:0.1mol " x="0.2mol"
根据电子守恒:4OH— — 4e—= 2H2O + O2↑
4 4mol 22.4L
n(OH—) 0.2mol V
4mol :0.2mol =22.4L: V=1.12L。n(H+)=n(OH—)="0.2mol" c(H+)=0.2mol/2.0L=0.1mol/L
 =-lgc(H+)=1.
=-lgc(H+)=1.
(2)用等质量的两块铜片代替石墨作电极,电极反应为:
阳极:Cu— 2e—=Cu2+ 阴极: Cu2+ + 2e— =" " Cu 根据转移电子守恒,阴极析出铜的质量和阳极溶解铜的质量相等,都是6.4g,电解后两铜片的质量相差为: 6.4g+6.4g=12.8g,溶液中c(H+)不变, 不变。
不变。
