问题
填空题
(8分)用双线桥标出下列反应中的电子转移的方向及数目,并指出氧化剂和还原剂
(1)3Cu+8HNO3===3Cu(NO3)2+2NO↑+4H2O
氧化剂是 ,还原剂是 ,
(2)2FeCl3+2HI=2FeCl2+2HCl+I2
氧化剂是 ,还原剂是
答案
(1)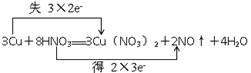 氧化剂是 HNO3,还原剂是 Cu
氧化剂是 HNO3,还原剂是 Cu
(2)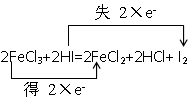 氧化剂是 FeCl3 ,还原剂是 HI
氧化剂是 FeCl3 ,还原剂是 HI
题目分析:(1)根据方程式可知,铜元素的化合价从0价升高到+2价失去2个电子,铜是还原剂。硝酸支氮元素的化合价从+5价降低到+2价,得到3个电子,硝酸做氧化剂。
(2)铁元素的化合价从+3价降低到+2价,得到1个电子,氯化铁是氧化剂。碘化氢中碘元素的化合价从-1价升高到0价,失去1个电子,做还原剂。
点评:物质失去电子,所含元素化合价升高的做还原剂,反之得到电子,物质所含元素化合价降低的做氧化剂,据此可以进行有关判断和计算。
