问题
选择题
结合下图判断,下列叙述正确的是
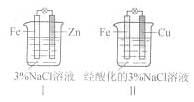
A.Ⅰ是验证牺牲阳极的阴极保护法的实验装置
B.Ⅰ和Ⅱ中负极反应均是Fe-2e-=Fe2+
C.Ⅰ和Ⅱ中正极反应均是O2+2H2O+4e-=4OH-
D.Ⅰ和Ⅱ中分别加入少量K3Fe(CN)6溶液,均有蓝色沉淀
答案
答案:A
装置I为中性溶液下的锌的吸氧腐蚀
正极:O2+2H2O+4e-=4OH-,负极:Zn-2e-=Zn2+
装置II为酸性情况下的铁铜原电池;
正极:2H++2e-=H2↑,负极:Fe-2e-=Fe2+
故:装置I是把铁做原电池的正极(阳极),得到保护,表述正确;而两装置中只有装置II中才会生成亚铁离子,故D选项错误。
