问题
填空题
(8分)下图是探究不同条件下化学能转变为电能的装置。请回答下列问题:
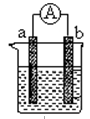
(1)当电极a为Al、电极b为Cu、电解质溶液为稀硫酸时,负极的电极反应式为: 。如果一电极质量减轻5.4 g,则另一极放出气体的体积为 L(标准状况)。
(2)燃料电池的工作原理是将燃料和氧化剂(如O2)反应所放出的化学能直接转化为电能。现设计一燃料电池,以电极a为正极,电极b为负极,氢气为燃料,采用KOH溶液为电解液;则氢气应通入 极(填a 或b,下同),电子从 极流出。
a 极发生电极反应式为:_____________________________。
答案
(1)Al-3e-= Al3+(2分) 6.72 L(2分)
(2) (2)b b (共2分,各1分) O2+2H2O+4e-=4OH- (2分)
Al---H2SO4-----Cu的原电池中铝做负极Al-3e-= Al3+,铜做正极2H++2 e-=H2,
燃料电池中还原剂为负极,氧化剂为正极,氢气为负极,电子从负极流到正极。(+)O2+2H2O+4e-=4OH-