甲醇可作为燃料电池的原料。以CH4和H2O为原料,通过下列反应来制备甲醇。
Ⅰ:CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH=206.0 kJ·mol-1
Ⅱ:CO(g)+2H2(g)=CH3OH(g) ΔH=-129.0 kJ·mol-1
(1)CH4(g)与H2O(g)反应生成CH3OH(g)和H2(g)的热化学方程式为______________________________________________________。
(2)将1.0 mol CH4和2.0 mol H2O(g)通入容积为100 L的反应室,在一定条件下发生反应Ⅰ,测得在一定的压强下CH4的转化率与温度的关系如右图。
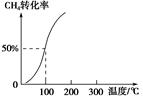
①假设100 ℃时达到平衡所需的时间为5 min,则用H2表示该反应的平均反应速率为________。
②100 ℃时反应Ⅰ的平衡常数为________。
(3)在压强为0.1 MPa、温度为300 ℃条件下,将a mol CO与3a mol H2的混合气体在催化剂作用下发生反应Ⅱ生成甲醇,平衡后将容器的容积压缩到原来的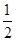 ,其他条件不变,对平衡体系产生的影响是________(填字母序号)。
,其他条件不变,对平衡体系产生的影响是________(填字母序号)。
A.c(H2)减少
B.正反应速率加快,逆反应速率减慢
C.CH3OH 的物质的量增加
D.重新平衡c(H2)/c(CH3OH)减小E.平衡常数K增大
(4)写出甲醇-空气-KOH溶液的燃料电池负极的电极反应式:__________________________________________________。
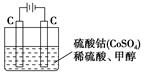
(5)甲醇对水质会造成一定的污染,有一种电化学法可消除这种污染,其原理是:通电后,将Co2+氧化成Co3+,然后以Co3+做氧化剂把水中的甲醇氧化成CO2而净化。实验室用如图装置模拟上述过程:
①写出阳极电极反应式____________________________。
②写出除去甲醇的离子方程式__________________________________。
(1)CH4(g)+H2O(g)=CH3OH(g)+H2(g) ΔH=77.0 kJ·mol-1
(2)①0.003 mol·L-1·min-1 ②2.25×10-4
(3)CD
(4)CH3OH-6e-+8OH-=CO32-+6H2O
(5)Co2+-e-=Co3+ 6Co3++CH3OH+H2O=CO2↑+6Co2++6H+
(1)写热化学方程式,注意聚集状态,目标反应可由反应Ⅰ、Ⅱ相加得到,计算出反应热。(2)计算速率和平衡常数时要注意容积的体积。计算H2的速率,
方法一:v(H2)=3v(CH4)=3×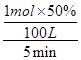 =0.003 mol·L-1·min-1,
=0.003 mol·L-1·min-1,
方法二:根据“三行式”
CH4(g)+ H2Og= CO(g)+3H2(g)
n(始)/mol 1.0 2.0 0 0
n(变)/mol 0.5 0.5 0.5 1.5
n(平)/mol 0.5 1.5 0.5 1.5
v(H2)=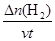 =
=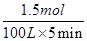 =0.003 mol·-1·min-1
=0.003 mol·-1·min-1
K=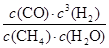 =
=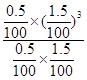 =2.25×10-4
=2.25×10-4
(3)体积压缩为原来的一半,则浓度变为原来的2倍,平衡的移动是个“减弱”的过程,浓度比原平衡大,A错误。压强增大,正逆反应速率均增大,B错误。压强增大,平衡向正反应方向移动,C、D正确。平衡常数只与温度有关,E错误。(4)负极上甲醇反应,KOH为电解质,产物为CO32-,“三步书写”。(5)阳极发生氧化反应,Co2+生成Co3+。Co3+将甲醇氧化,生成Co2+和CO2,注意溶液呈酸性。
