将镁、铝合金10.2 g 溶于4 mol·L-1的盐酸500 mL 里,若加入2 mol·L-1的氢氧化钠溶液,并使得沉淀达到最大量,则需加入此种氢氧化钠溶液为( )
A.1000 mL
B.500 mL
C.100 mL
D.1500 mL
答案:A
当镁铝合金溶于盐酸后,溶液中含有Al3+、Mg2+、H+,若与NaOH反应时,H+先反应,当沉淀量达到最大时,消耗NaOH的物质的量等于盐酸的物质的量,所以4 mol·L-1×0.5 L=2 mol·L-1×V,V=1 L=1000 mL,A项正确。

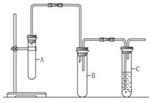
 -二氯乙烷已发生消去反应的现象是_______________,还可通过什
-二氯乙烷已发生消去反应的现象是_______________,还可通过什 么实验加以验证:________________________________________。
么实验加以验证:________________________________________。