问题
选择题
根据下图,下列判断中正确的是
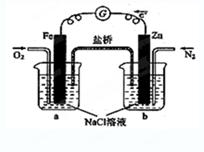
A.向烧杯a中加入少量K3[Fe(CN)6]溶液,有蓝色沉淀生成
B.烧杯b中发生反应为2Zn-4eˉ =2Zn2+
C.电子从Zn极流出,流入Fe极,经盐桥回到Zn极
D.烧杯a中发生反应O2 + 4H++ 4eˉ = 2H2O,溶液pH降低
答案
答案:B
题目分析:原电池中较活泼的金属是负极,失去电子,发生氧化反应。电子经导线传递到正极,所以溶液中的阳离子向正极移动,正极得到电子,发生还原反应。锌比铁活泼,据此可知,锌是负极,失去电子,生成锌离子。铁是正极,溶液中的氧气得到电子,所以选项A不正确,得不到蓝色沉淀,B正确;C不正确,电子不可能在溶液中传递,只能在外电路通过导线传递。D不正确,溶液显中性,氧气得到电子生成OH-,答案选B。
