(18分)为验证氧化性Cl2>Fe3+>SO2,某小组用下图所示装置进行实验(夹持仪器和 A中加热装置已略,气密性已检验)实验过程如下:
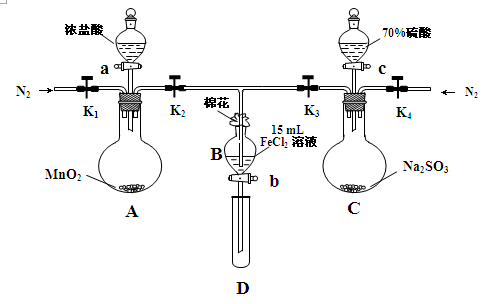
Ⅰ.打开弹簧夹K1~K4,通入一段时间N2,再将T型导管插入B中,继续通入N2,然后关闭K1、K3、K4。
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热。
Ⅲ.当B中溶液变黄时,停止加热,夹紧弹簧夹K2。
Ⅳ.打开活塞b,使约2mL的溶液流入D试管中,检验其中的离子。
Ⅴ.打开弹簧夹K3、活塞c,加入70%的硫酸,一段时间后夹紧弹簧夹K3。
Ⅵ.更新试管D,重复过程Ⅳ,检验B溶液中的离子。
(1)过程Ⅰ的目的是_________________________________________________。
(2)棉花中浸润的溶液为______________________。
(3)A中发生反应的化学方程式为 。
(4)用70%的硫酸制取SO2,反应速率比用98%的硫酸快,原因是 。
(5)能说明氧化性Fe3+>SO2的离子方程式是______________________________________。
(6)甲、乙、丙三位同学分别完成了上述实验,他们的检测结果一定能够证明氧化性Cl2>Fe3+>SO2的是 (填“甲”“乙”“丙”)。
| 过程Ⅳ B溶液中含有的离子 | 过程Ⅵ B溶液中含有的离子 | |
| 甲 | 有Fe3+无Fe2+ | 有SO42- |
| 乙 | 既有Fe3+又有Fe2+ | 有SO42- |
| 丙 | 有Fe3+无Fe2+ | 有Fe2+ |
颜色变为浅绿色。
查阅资料:Fe2+(aq)+SO32-(aq) FeSO3(s)(墨绿色)
FeSO3(s)(墨绿色)
提出假设:FeCl3与SO2的反应经历了中间产物FeSO3,溶液的红棕色是FeSO3(墨绿色)与FeCl3(黄色)的混合色。某同学设计如下实验,证实该假设成立:
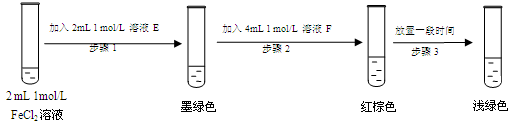
①溶液E和F分别为 、 。
②请用化学平衡原理解释步骤3中红棕色溶液颜色变为浅绿色的原因 。
(1)排除空气(1分) (2)NaOH溶液 (3)MnO2 + 4HCl(浓) △MnCl2+Cl2↑+ 2H2O
(4)70%H2SO4中c(H+)大 (5)2Fe3+ + SO2 + 2H2O=2Fe2+ + SO42-+4H+ (6)乙、丙
(7)① Na2SO3溶液 、FeCl3溶液
②Fe3+ 消耗 SO32-,c(SO32-)减小,使平衡Fe2+(aq)+SO32-(aq) FeSO3(s)逆向移动,溶液颜色由红棕色变为浅绿色。(3分)
FeSO3(s)逆向移动,溶液颜色由红棕色变为浅绿色。(3分)
题目分析:(1)打开K1~K4,关闭K5、K6,通入一段时间N2,目的是排出装置中的氧气。
(2)氯气、二氧化硫有毒,棉花中浸有NaOH溶液,吸收多余氯气、二氧化硫,防止污染空气。
(3)A中发生二氧化锰与浓盐酸的反应,生成氯化锰、氯气、水,该反应为MnO2 + 4HCl(浓) △MnCl2+Cl2↑+ 2H2O。
(4)因氢离子浓度越大,反应速率越快,则70%的硫酸中的氢离子浓度比98%的硫酸中的氢离子浓度大,所以反应速率快。
(5)铁离子能把二氧化硫氧化生成硫酸,反应的离子方程式为2Fe3+ + SO2 + 2H2O=2Fe2+ + SO42-+4H+。
(6)乙中第一次,说明氯气不足,氯气氧化性大于铁离子,第二次有硫酸根离子,说明发生二氧化硫与铁离子的反应,则氧化性铁离子大于二氧化硫丙中第一次有Fe3+,无Fe2+,则氯气的氧化性大于铁离子,第二次有亚铁离子,说明发生二氧化硫与铁离子的反应,则氧化性铁离子大于二氧化硫,故答案为:乙、丙。
(7)①E与氯化亚铁溶液反应产生墨绿色,说明反应中有亚硫酸亚铁生成,因此E应该是Na2SO3溶液。根据FeSO3(墨绿色)与FeCl3(黄色)的混合后溶液显红棕色可知,F应该是FeCl3溶液。
②铁离子具有氧化性,因此Fe3+ 消耗 SO32-,导致c(SO32-)减小,使平衡Fe2+(aq)+SO32-(aq) FeSO3(s)逆向移动,溶液颜色由红棕色变为浅绿色。
FeSO3(s)逆向移动,溶液颜色由红棕色变为浅绿色。
