某无色溶液X,由Na+、Ag+、Ba2+、Al3+、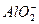 、
、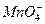 、
、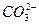 、
、 中的若干种离子组成,取溶液进行如下连续实验:
中的若干种离子组成,取溶液进行如下连续实验:
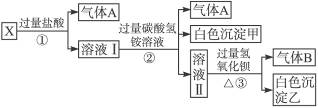
(1)气体A的成分是______________,气体B的成分是_______________。(填化学式)
(2)X溶液中一定存在的离子是_______________。
(3)写出步骤①中发生反应的所有的离子方程式_______________。
(4)写出步骤②中形成白色沉淀甲的离子方程式_______________。
(5)通过上述实验,白色沉淀乙的组成可能是_______________;只要设计一个简单的后续实验就可以确定该沉淀的组成,该方法是______________________________。
(1)CO2NH3
(2)Na+、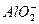 、
、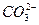
(3)C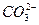 +2H+====CO2↑+H2O
+2H+====CO2↑+H2O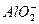 +4H+====Al3++2H2O
+4H+====Al3++2H2O
(4)Al3++3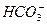 ====Al(OH)3↓+3CO2↑
====Al(OH)3↓+3CO2↑
(5)BaCO3或BaCO3、BaSO4的混合物在沉淀乙中加足量的稀盐酸,若全部溶解则说明只有BaCO3,若不能全部溶解,说明是BaCO3和BaSO4的混合物
由溶液是无色的排除了 的干扰,能和盐酸反应生成气体的是
的干扰,能和盐酸反应生成气体的是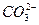 ,
,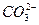 的存在排除了Ag+、Ba2+、Al3+,所以原溶液中含有的阳离子只能是Na+。与碳酸氢铵溶液反应生成白色沉淀的离子只能是Al3+(由原溶液中的
的存在排除了Ag+、Ba2+、Al3+,所以原溶液中含有的阳离子只能是Na+。与碳酸氢铵溶液反应生成白色沉淀的离子只能是Al3+(由原溶液中的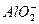 与过量的盐酸反应而得),所以原溶液中含有
与过量的盐酸反应而得),所以原溶液中含有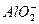 ,沉淀甲只能为Al(OH)3,发生步骤①的反应为:
,沉淀甲只能为Al(OH)3,发生步骤①的反应为: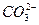 +2H+====CO2↑+H2O和
+2H+====CO2↑+H2O和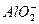 +4H+====Al3++2H2O;步骤②时形成白色沉淀甲的离子方程式为Al3++3
+4H+====Al3++2H2O;步骤②时形成白色沉淀甲的离子方程式为Al3++3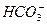 ====Al(OH)3↓+3CO2↑;过量的Ba(OH)2提供了大量的OH-和Ba2+,所以气体B为NH3,白色沉淀乙可能是BaCO3或BaCO3、BaSO4的混合物,不好确定,检验方法为在沉淀乙中加足量的稀盐酸,若全部溶解则说明只有BaCO3,若不能全部溶解,说明是BaCO3和BaSO4的混合物。
====Al(OH)3↓+3CO2↑;过量的Ba(OH)2提供了大量的OH-和Ba2+,所以气体B为NH3,白色沉淀乙可能是BaCO3或BaCO3、BaSO4的混合物,不好确定,检验方法为在沉淀乙中加足量的稀盐酸,若全部溶解则说明只有BaCO3,若不能全部溶解,说明是BaCO3和BaSO4的混合物。
