某溶液甲中可能含有下列离子中的几种:K+、NO 、SO
、SO 、NH
、NH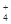 、CO
、CO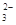 (不考虑溶液中由水电离的少量的H+和OH-),取200mL该溶液,分为两等份进行下列实验:
(不考虑溶液中由水电离的少量的H+和OH-),取200mL该溶液,分为两等份进行下列实验:
实验1:第一份加入足量的烧碱并加热,产生的气体在标准状况下为672mL;
实验2:第二份先加入足量的盐酸,无现象,再加入足量的BaCl2溶液,得固体2.33g。
(1)甲溶液中一定存在的离子是 ;
(2)甲溶液中一定不存在的离子是 ;
(3)甲溶液中可能存在的离子是 ;你得出此结论的理由是 。
(1)NO 、SO
、SO 、NH
、NH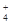 (2)CO
(2)CO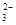
(3)K+ 由题意知:溶液中含NH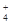 0.03mol,SO
0.03mol,SO 0.01mol,据电中性原理,必有NO
0.01mol,据电中性原理,必有NO ,若NO
,若NO 为0.01mol,则无K+,若NO
为0.01mol,则无K+,若NO 大于0.01mol,则有K+。
大于0.01mol,则有K+。
题目分析:(1)根据实验1:第一份加入足量的烧碱并加热,因NH4++OH-=NH3↑+H2O,会产生标准状况下为224mL气体,证明含有NH4+,且物质的量为0.01mol;
实验2:第二份先加入足量的盐酸,无现象,则一定不含有CO32-,再加足量的BaCl2溶液,得固体2.33g,证明一定含有SO42-,且物质的量为:n="m/M" ="2.33g/233g/mol" =0.01mol;根据溶液中的电荷守恒,溶液呈电中性,则一定含有钾离子,且钾离子的浓度≥0.01mol×2−0.01mol× 0.1L ═0.1mol/L,所以该溶液中肯定含有NH4+、S042-、K+,
故答案为:K+、NH4+、S042-;
(2)实验2:第二份先加入足量的盐酸,无现象,则不含有CO32-,如果有CO32-,CO32-+2H+=H2O+CO2↑,会有二氧化碳气体产生,故答案为:CO32-;
(3)根据(1)知:钾离子的浓度≥0.01mol×2−0.01mol ×0.1L =0.1mol/L,如果K+的物质的量等于0.01mol,则不含NO3-,如果K+的物质的量大于0.01mol,则还应含有NO3-,
故答案为:NO3-;由题意知,NH4+物质的量为0.01mol,SO42-物质的量为0.01mol,根据溶液呈电中性原理,应该含有K+,如果K+的物质的量等于0.01mol,则不含NO3-,如果K+的物质的量大于0.01mol,则还应含有NO3-.
