问题
选择题
据报道,最近摩托罗拉公司研发了一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量可达现在使用的镍氢电池或锂电池的十倍,可连续使用一个月才充一次电.其电池反应为:2CH3OH+3O2+4OH-
2CO32-+6H2O,则下列说法错误的是( )放电 充电
A.放电时CH3OH参与反应的电极为正极
B.充电时电解质溶液的pH逐渐增大
C.放电时负极的电极反应为:CH3OH-6e-+8OH-=CO32-+6H2O
D.充电时每生成1molCH3OH转移6mol电子
答案
A、放电时,相当于原电池的工作原理,负极发生失电子的氧化反应,根据总反应:2CH3OH+3O2+4OH-
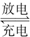
2CO32-+6H2O,则放电时CH3OH参与反应的电极为负极,故A错误;
B、充电时,相当于电解池的工作原理,根据总反应:2CH3OH+3O2+4OH-
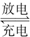
2CO32-+6H2O,生成大量的氢氧根离子,所以碱性增强,故电解质溶液的pH逐渐增大,故B正确;
C、放电时负极发生失电子的氧化反应,根据总反应:2CH3OH+3O2+4OH-
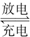
2CO32-+6H2O,则负极的电极反应为:CH3OH-6e-+8OH-=CO32-+6H2O,故C正确;
D、充电时,根据总反应:2CH3OH+3O2+4OH-
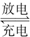
2CO32-+6H2O,每生成2molCH3OH转移12mol电子,则每生成1mol
CH3OH转移6mol电子,故D正确.
故选A.
