(Ⅰ)原电池是一种将______能转化为电能的装置.如图所示的原电池中,锌片上发生______反应(填“氧化”或“还原”).
(Ⅱ)Li-SOCl2电池可用于心脏起搏器.该电池的电极材料分别为锂和碳,电解液是LiAlCl4-SOCl2.电池的总反应可表示为:4Li+2SOCl2=4LiCl+S+SO2.请回答下列问题:
(1)电池的负极材料是______
(2)电池正极发生的电极反应为______;
(3)组装该电池必须在无水、无氧的条件下进行,原因是______.
(4)SOCl2易挥发,实验室中常用NaOH溶液吸收SOCl2,生成Na2SO3和NaCl. 如果把少量水滴到SOCl2中,实验现象是______,反应的化学方程式为______.
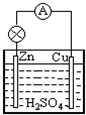
(Ⅰ)原电池是把化学能转变成电能的装置;该原电池中锌片作负极,负极上失电子,发生氧化反应.
故答案为:化学; 氧化;
(Ⅱ)(1)锂的活泼性大于碳的,所以锂作负极.
故答案为:锂;
(2)正极上得电子发生还原反应,根据反应方程式知,SOCl2得电子生成Cl-、S、SO2.
故答案为:2SOCl2+4e-=4Cl-+S+SO2
(3)锂和钠是同一主族的元素,性质具有相似性,钠和空气中的氧气、水蒸气反应,所以锂和空气中的氧气、水蒸气也能反应;SOCl2也可与水反应,所以组装该电池必须在无水、无氧的条件下进行.
故答案为:锂是活泼金属,易与H2O、O2反应;SOCl2也可与水反应.
(4)由NaOH和SOCl2生成Na2SO3和NaCl两种盐知,SOCl2和水生成酸或酸性氧化物,根据原子守恒得,SOCl2和水生成
SO2和HCl,二氧化硫有刺激性气味,HCl遇水蒸气形成小液滴出现白雾,所以实验现象是出现白雾,有刺激性气体生成.
故答案为:出现白雾,有刺激性气体生成; SOCl2+H2O=SO2↑+2HCl↑.
